Das Daniell-Element
Das Daniell-Element hat aktuell keine technische oder praktische Bedeutung mehr, wird aber trotzdem in Schule und Universität oft zum Einstieg in das Themenfeld "Batterien und Akkus" bzw. galvanische Zellen benutzt, weil es so wunderbar einfach zu verstehen ist.
Das Daniell-Element ist eine sehr einfache Batterie, die nach den gleichen Prinzipien funktioniert wie alle Batterien und Akkus, die derzeit technisch eingesetzt werden. Lithiumionenakkus, Lithium-Eisenphosphat-Akkus, Alkali-Mangan-Batterien, ... nutzen alle das gleiche Funktionsprinzip und bestehen aus den gleichen Bauteilen wie das Daniell-Element; lediglich die verwendeten Stoffe sind andere.
Aufbau des Daniell-Elements

Das Daniell-Element besteht aus zwei Halbzellen, einer Kupferhalbzelle aus einer Kupferelektrode, d.h. einem Kupferblech, die in eine wässriger Kupfersulfat-Lösung eintaucht. Die Zweite Halbzelle besteht aus einer Zinkelektrode in einer Zinksulfatlösung.
Die beiden Halbzellen sind durch eine "semipermeable" Membran getrennt. Semipermeable bedeutet Teildurchlässig. Die Membran ist also eine für einige Stoffe durchlässig und für Andere undurchlässig.
In der Abbildung ist zwischen den beiden Blechen ein Voltmeter dargestellt, dass eine Spannung von etwa 1,1 V anzeigen würde.
Erklärung
Beim Daniell-Element tauchen die beiden Elektroden aus Kupfer und Zink jeweils in wässrige Lösungen eines Salzes eben dieser Metalle. Um verstehen zu können, wie das Daniell-Element "Strom" liefert, müssen wir uns zunächst angucken, was in den Lösungen ist.
Metallsalze in Wasser
Beim Lösen in Wasser dissoziieren die Salze (vgl. Ionenbindung) in freie, aquotisierte Ionen. Dissoziieren bedeutet "auseinander gehen" - die Anionen und Kationen der Salze werden dabei von Wassermolekülen eingehüllt (aquotisiert) und sind danach unabhängig voneinander im Wasser weitestgehend frei beweglich.
ZnSO4 → Zn2+(aq) + SO42-(aq)
CuSO4 → Cu2+(aq) + SO42-(aq)
Die Lösung des Kupfersulfats enthält demnach frei bewegliche Kupferionen (Cu2+) und die des Zinksulfats frei bewegliche Zinkionen (Zn2+). Jede der beiden Metallelektroden taucht in eine Lösung ein, die eben dieses Metall in seiner oxidierten Form enthält.
Ausbildung eines elektrochemischen Potenzials
Zwischen der oxidierten Form des Metalls (Cu2+ bzw. Zn2+) und seiner reduzierten Form (Cu bzw. Zn) in Form der Metallelektroden stellt sich nun ein Gleichgewicht ein, bei dem Elektronen mit dem "Elektrodenkörper" ausgetauscht werden:
Cu ⇄ Cu2+(aq) + 2 e-
Zn ⇄ Zn2+(aq) + 2 e-
Hierbei stehen die Metallatome des festen Metalls mit den in Wasser gelösten Ionen im Gleichgewicht. Die Elektronen werden jeweils mit dem "Elektrodenkörper" ausgetauscht, weshalb sich die "Elektronendichte" im Metall durch die Einstellung des Gleichgewichtes ändert.
Manche Schulbücher sprechen von einem "Lösungsdruck" und meinem damit das Bestreben des festen Metalls als Ion in Lösung zu gehen und dabei seine Elektronen im "Elektrodenkörper" zurückzulassen. Dem Lösungsdruck entgegen wirkt in dieser Betrachtungsweise der sogenannte "Abscheidungsdruck". Damit wird das Bestreben der Metallionen beschrieben, aus dem Elektrodenkörper Elektronen aufzunehmen und als Metallatom Teil des festen Elektrodenkörpers zu werden.
| Lösungsdruck | Abscheidungsdruck | |
|---|---|---|
| Kupfer | Cu → Cu2+(aq) + 2 e- | Cu2+(aq) + 2 e- → Cu |
| Zink | Zn → Zn2+(aq) + 2 e- | Zn2+(aq) + 2 e- → Zn |
Wenn Lösungs- und Abscheidungsdruck gleich groß sind, sind Hin- und Rückreaktion gleich schnell und es stellt sich ein dynamisches Gleichgewicht ein (vgl. chemisches Gleichgewicht, Reaktionsgeschwindigkeit und Massenwirkungsgesetz), wie schon zu Beginn dieses Abschnitts beschrieben.
Da die Elektronen immer mit dem "Elektrodenkörper" ausgetauscht werden, beeinflusst die Einstellung des Gleichgewichts aus Lösungs- und Abscheidungsdruck die Elektronendichte im "Elektrodenkörper". Wenn die Dichte der negativen Elektronen dabei gegenüber dem "normalen" Zustand erhöht wird, ist der Elektrodenkörper negativ geladen. Es stellt sich ein "negatives Elektrodenpotenzial" ein. Ist die Elektronendichte hingegen gegenüber dem "normalen" Zustand verringert, stellt sich ein "positives Elektrodenpotenzial" ein.
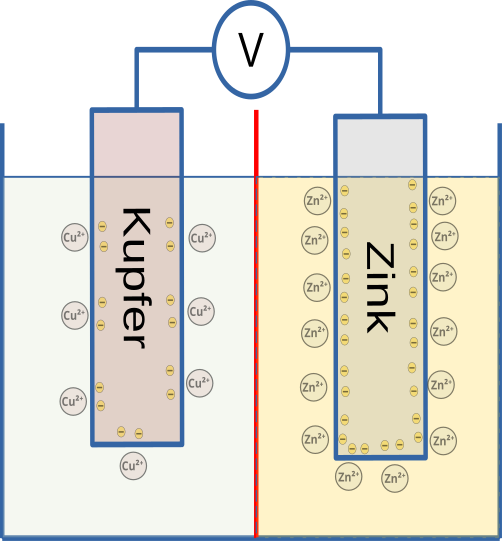
Da Kupfer edler als Zink ist (vgl. Edle und unedle Elemente), ist der Lösungsdruck des Kupfers kleiner als der des Zinks und der Abscheidungsdruck der Kupferionen ist größer als der der Zinkionen. Der Grund ist, dass das edlere Kupfer schwerer oxidiert und leichter reduziert wird als das unedlere Zink. Das Elektrodenpotezial der Kupferelektrode ist deshalb größer als das der Zinkelektrode. Zwischen den beiden Elektroden bildet sich eine Potenzialdifferenz, eine Spannung, aus.
Ursache der Spannung ist die gegenseitige Abstoßung der negativ geladenen Elektronen. Die elektrische Ladung strebt wegen der Abstoßung gleicher Ladungen eine möglichst gleichmäßige Verteilung an. D.h. die überzähligen Elektronen im Zinkblech werden zum Kupferblech "gedrückt".
Stromfluss - wenn Elektronen der Spannung folgen
Wenn man den Elektronen nun die Möglichkeit gibt, der Spannung zu folgen, indem im Stromkreis das Voltmeter etwa durch eine Glühlampe ausgetauscht wird, werden sich die Elektronen vom Ort hoher Elektronendichte zum Ort geringerer Elektronendichte bewegen. Bei diesem Stromfluss transportieren sie eine Energie von 1,1V=1,1J/C durch den Stromkreis. Diese Energie können sie an den Verbraucher, also z.B. eine Glühlampe abgeben, die dann (schwach) leuchten wird.
Durch den Stromfluss nimmt dann die Elektronendichte im Zinkblech ab und die im Kupferblech zu, was ziemlich schnell zu einer deutlich geringeren Potenzialdifferenz und dann auch sehr schnell zum Ende des Elektronenflusses führen würde.
Allerdings wird durch die Wegnahme von Elektronen aus dem Zinkblech das Gleichgewicht
Zn ⇄ Zn2+(aq) + 2 e-
in der Weise beeinflusst, dass ständig neue Zinkionen und Elektronen nachgebildet werden, da man eines der Reaktionsprodukte, die Elektronen, aus dem Gleichgewicht entfernt. In der gleichen Weise wird in der Kupferhalbzelle das Gleichgewicht
Cu ⇄ Cu2+(aq) + 2 e-
durch die kontinuierliche Elektronenzufuhr in der Weise beeinflusst, dass die zusätzlichen Elektronen mit den Kupferionen aus der Lösung zu metallischem Kupfer reagieren. Durch diese Gleichgewichtsverschiebungen wird die Potenzialdifferenz dauerhaft aufrecht erhalten, sodass kontinuierlich eine Spannung von knapp unter 1,1V erhalten bleibt, die für einen kontinuierlichen Stromfluss sorgt - zumindest, wenn die semipermeable Membran tut, was sie soll.
Ionenstrom zum Ladungsausgleich - die semipermeable Membran
Bei dem gerade beschriebenen Stromfluss laufen in den beiden Halbzellen kontinuierlich die folgenden Reaktionen ab:
Zn → Zn2+(aq) + 2 e-
Cu2+(aq) + 2 e- → Cu
In der Lösung rund um das Zinkblech befinden sich also immer mehr Kationen und in der rund um die Kupferelektrode immer weniger. Der Überschuss an positiven Ionen in der Zinkhalbzelle und der durch die zurückbleibenden Sulfationen gebildete Überschuss an negativen Ionen in der Kupferhalbzelle steht dem Elektronenfluss entgegen und würde den Stromfluss praktisch sofort beenden. Deshalb muss mit dem Elektronenfluss durch den Verbraucher gleichzeitig ein Fluss der Zinkionen durch die semipermeable Membran erfolgen, um die Ladungsunterschiede auszugleichen.
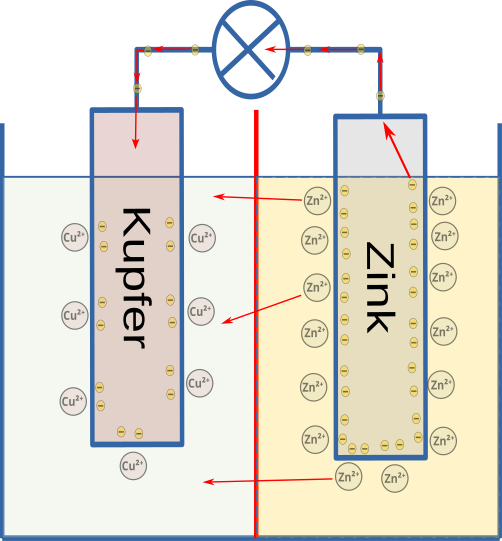
Als Alternative zum Zinkionenstrom wäre auch ein Strom der Sulfationen (SO42-) aus der Kupferhalbzelle in die Zinkhalbzelle möglich. Allerdings würde hierdurch die Salzkonzentration in der Zinkhalbzelle insgesamt immer größer. Ein Strom der Zinkionen in die Kupferhalbzelle ist daher besser, denn die Salzkonzentrationen in beiden Lösungen bleiben dabei insgesamt unverändert.
Zum Ladungsausgleich zwischen den Lösungen gibt es also zwei Möglichkeiten. Für immer zwei Elektronen, die durch das Kabel von der Zink- in die Kupferhalbzelle fließen bewegt sich gleichzeitig ...
- ... ein doppelt positiv geladenes Zinkion in die gleiche Richtung oder
- ... ein doppelt negativ geladenes Sulfation in die Gegenrichtung...
...durch die semipermeable Membran.
In jedem Fall muss die semipermeable Membran den direkten Kontakt zwischen Oxidationsmittel (hier Kupferionen) und Reduktionsmittel (hier metallisches Zink) verhindern. Täte sie dies nicht, könnten die Kupferionen direkt an der Oberfläche des Zinks das Zink oxidieren und die Elektronen müssten nicht mehr den Weg durch den äußeren Stromkreis nehmen. Die Batterie hätte einen inneren Kurzschluss und wäre defekt.
Gesamtreaktion
Wenn Strom durch den äußeren Stromkreis fließt, reagieren die Kupferionen aus der Kupferhalbzelle mit dem metallischen Zink in der Zinkhalbzelle in folgender Redoxreaktion:
Cu2+(aq) + Zn → Zn2+(aq) + Cu
Bei dieser Reaktion werden zwei Elektronen von einem Zinkatom zu einem Kupferion übertragen. Die Reaktion ist insgesamt exotherm und läuft sie freiwillig ab. Die bei der Reaktion freiwerdende Energie steht dabei als elektrische Energie im Stromkreis zur Verfügung; sie wird also von den beiden Elektronen durch den Stromkreis zum Verbraucher transportiert.
Energie- und Stoffumsatz
Wenn das Daniell-Element als "Batterie" benutzt wird, um einen elektrischen Verbraucher mit Energie zu versorgen, wird chemische Energie bei der Reaktion in elektrische Energie umgewandelt.
Energieumsatz
Das Daniell-Element liefert eine Spannung von 1,1 V. Spannung ist definiert als Energie pro Ladung, d.h. pro Coulomb übertragener elektrischer Ladung werden demnach 1,1 Joule Energie freigesetzt.

Jedes Elektron trägt die gleiche, sehr kleine Ladung. 1 mol Elektronen trägt dann wegen der großen Zahl "1 mol" tatsächlich eine ziemlich große elektrische Ladung von 96485,3 C. Dies wird durch die Faraday-Konstante F ausgedrückt: F = 96485,3 C/mol
Mit der Faraday-Konstante und der obigen Definition der Spannung lässt sich auf einfache Weise der molare Energieumsatz der Reaktion zwischen Kupferionen und metallischem Zink ausrechnen.
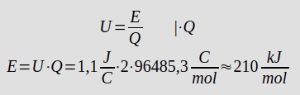
Da pro Kupferion und auch pro Zinkatom zwei Elektronen übertragen werden, ist die bei einem Mol Stoffumsatz übertragene Ladung das doppelte der Faraday-Konstante. Die Reaktion zwischen Kupferionen und Zinkatomen ist somit mit ca. 210 kJ/mol exotherm.
Cu2+(aq) + Zn → Zn2+(aq) + Cu ; ΔRH = -210 kJ/mol
Stoffumsatz
Aus der Reaktionsgleichung zuvor kann man erkennen, dass für jedes Kupferion auch in Zinkatom reagieren muss und dabei dann bei einem Mol Stoffumsatz 210 kJ Energie frei werden. Mit den molaren Massen von Zink (65,39 g/mol) und Kupfer (63,55 g/mol) ergibt sich dann für die 210 kJ Energieertrag folgender Massenumsatz:
Kupferionen: m = n · M = 1 mol · 63,55 g/mol = 63,55 g
Zink: m = n · M = 1 mol · 65,39 g/mol = 65,39 g
Da 210 kJ eine etwas schwierig vergleichbare Energieportion ist, rechnen wir mal auf 1 kWh hoch. 1 kWh sind 3.600 kJ. Damit ergibt sich ein auf die Kilowattstunde bezogener Stoffumsatz von:
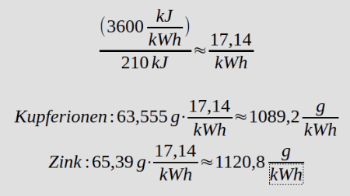
Das Daniell-Element müsste demnach für 1 kWh elektrischer Energie mindestens 1,1 kg Kupferionen und zusätzlich etwas mehr Zink enthalten. Dazu kämen die mit den Kupferionen zwingend enthaltenen Anionen sowie der wässrige Elektrolyt. Mit dann vielleicht etwa 3 kg "Aktivmaterial" plus Lösungsmittel je Kilowattstunde elektrischer Energie wäre das Daniell-Element insgesamt gar nicht mal schlecht. Allerdings dürfte sich rein technisch niemals das gesamte "Aktivmaterial" energetisch nutzen lassen und außerdem wäre das Daniell-Element nach wie vor nicht wiederaufladbar! Außerdem ändert sich die Spannung des Daniell-Elements relativ stark mit dem "Ladestand", was es für technische Anwendungen eher unattraktiv macht.
